对于需要选购多肽的老师同学们来说,选择合适的多肽纯度对实验和钱包都大有裨益。常常在进行某个实验时,我们会面临这样的困惑:不知道需要选择多高纯度的多肽。如果纯度过低,实验效果可能不尽如人意;而如果纯度过高,又可能让钱包承受不了。为方便大家实验的进行,这里将介绍多肽纯度相关知识以及不同纯度的选择指南。
1、多肽纯度与净含量
可能有小伙伴会疑惑,纯度究竟是什么?是多肽的净含量吗?其实,纯度和净含量是两个不同的概念。
纯度定义的是多肽样品中含正确序列组分的百分比,通常由高效液相色谱测定。在合成多肽链过程中,肽键的形成并非总是完美的,因此并非每一条生成多肽链都能完全符合预定的目标序列,这些“错误”多肽链混杂在合成的产物中并占据一定的比例。
肽的净含量则是指样品中肽类物质相对于非肽类物质所占的百分比。冻干多肽的重量中不仅包含多肽本身,还包含一些非肽的组份,如水、被吸收的溶剂和盐等。肽的净含量通常通过氨基酸组分分析或氮元素分析法来测定。
2、影响纯度的杂质
线性肽链常用Fmoc固相合成法延长,一般是利用受Fmoc保护的氨基酸从C端向N端逐步连接。具体反应包括树脂溶胀、缩合氨基酸、脱保护、重复缩合、裂解。如果每一步都能100%完成,
则会得到一个全长的多肽,但这很难实现。因为无论方案如何优化,总会有反应未完全和存在副反应的情况,从而产生杂质,影响多肽的纯度。
2.1杂质来源
多肽的杂质来源可分为三类:一是由起始物料引入,二是由生产工艺副反应产生,三是长期放置过程中降解产生。
树脂和保护氨基酸会影响多肽纯度。以Fmoc保护氨基酸为例,常见的杂质包括保护不完全氨基酸、手性异构体、同分异构体、二肽衍生物、β-丙氨酸杂质等,这些杂质会随着合成过程而加入到多肽中。
在生产和存放过程中产生的杂质包括缺失肽、插入肽、错结肽、差向肽、Asn/Gln脱酰胺产物、消旋杂质、氧化杂质、水解杂质、聚合物开环杂质以及开环后的重组杂质、剪切和纯化过程中的副产品、
反应试剂和溶剂、金属催化剂、缩合剂等残留物等。
这些杂质在不同程度上可能对多肽的应用产生显著影响。
1.影响实验结果:特定的错误序列可能干扰目标结合的研究,而三氟乙酸(TFA)等溶剂可能对生物检测中的细胞具有毒性。
2.影响多肽的生物活性:错误的序列或氧化等化学修饰可能显著降低多肽的生物活性。
3.增加实验的复杂性:需要额外的步骤来识别和去除杂质。
4.降低多肽的稳定性:某些杂质可能促进多肽的降解或聚集。
5.影响药物开发的安全性和有效性:多肽药物中的杂质(有关物质)还会影响药物的安全性和疗效,因此在药物开发中,高纯度的多肽是必需的。
2.3优化
为减少杂质的影响,首先需要对合成过程和添加剂进行优化,确保合成的分子序列正确率足够高,同时将错误合成的序列降至最低。其次,对合成后的下游处理步骤进行优化,如合成后盐交换步骤,
以去除合成过程中引入的盐类杂质。此外,还应评估肽在溶液中的稳定性以及减少冷冻干燥过程中的冻干损伤。
3、不同纯度肽的实验应用指南
在多肽的实验中,究竟应选择多高的纯度?是越高越好吗?一般来说,对于同样的序列和数量的多肽,纯度越高,单位质量的多肽价格也就越高,所需时间也就越长。
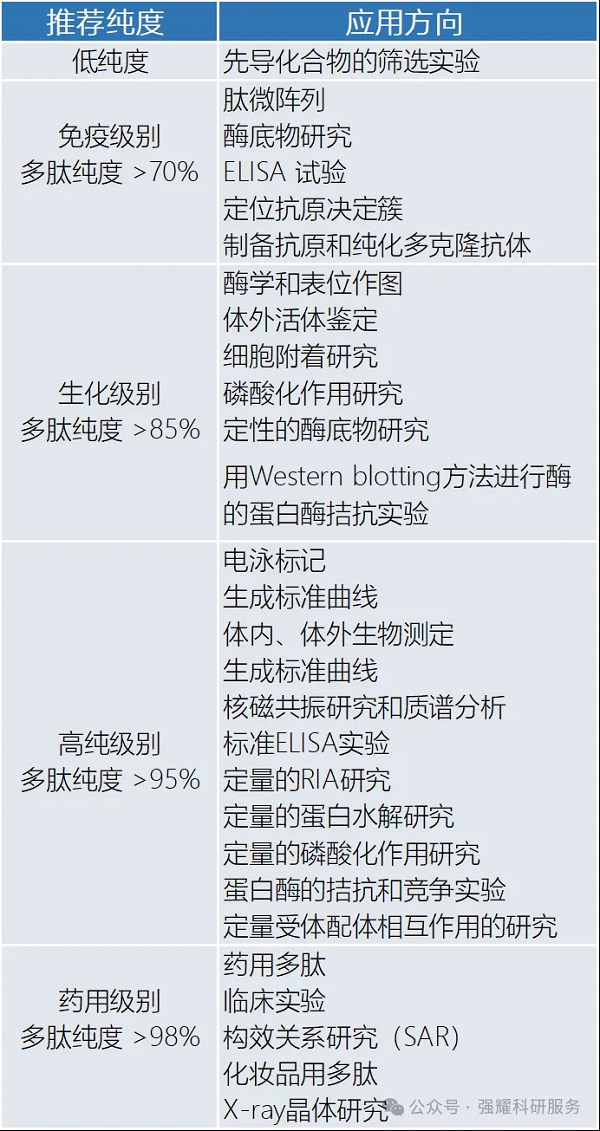
因此,一般应根据实验目的选择合适的多肽纯度。大于70%纯度的多肽通常用于制备和检测抗体,大于85%纯度的多肽通常用于酶和生物学活性的研究,大于95%纯度的多肽能极好地满足定量分析的要求。具体实验可参考以下表格。


 联系我们
联系我们
 返回
返回