上海长征医院消化内科的谢渭芬研究团队发表了一项重要研究成果,揭示了SOX9蛋白在YAP(Yes-Associated Protein)激活过程中的关键作用。这项研究不仅加深了我们对细胞核转运机制的理解,还为开发新的抗癌疗法提供了理论基础。
该研究发表在影响因子为40.8的《Signal Transduction and Targeted Therapy》期刊上,题为“SRY-Box transcription factor 9 triggers YAP nuclear entry via direct interaction in tumors”
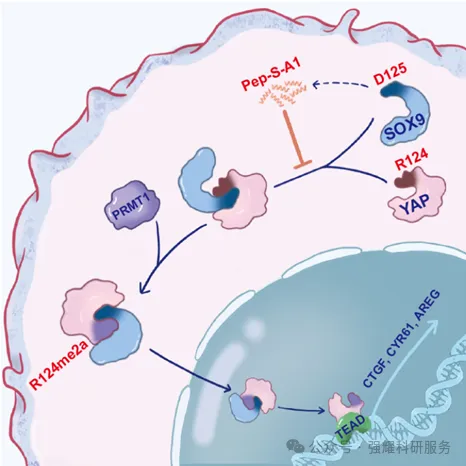
SOX9 通过直接相互作用触发 YAP 核进入的机制示意图
1、研究背景与发现
YAP蛋白是一种重要的转录共激活因子,在细胞增殖和组织发育过程中发挥着关键作用。当YAP位于细胞核内时,它可以激活一系列与细胞生长相关的基因,从而促进肿瘤的发生和发展。然而,YAP如何从细胞质转运到细胞核的具体机制一直不甚清楚。本研究首次揭示了SOX9蛋白在这一过程中的重要作用。
关键发现
1.SOX9促进YAP核转运
研究人员发现,SOX9能够通过直接相互作用促进YAP从细胞质转移到细胞核。具体来说,SOX9蛋白的第125位天冬氨酸(Asp-125)与YAP蛋白的第124位精氨酸(Arg-124)之间存在特异性结合。这种结合对于YAP的核转位至关重要
进一步研究表明,蛋白质精氨酸甲基转移酶1(PRMT1)催化YAP蛋白第124位精氨酸(YAP-R124)的不对称二甲基化,可以增强YAP与SOX9的结合能力。这一发现揭示了YAP核转位调控的一个新机制,并与多种癌症的不良预后密切相关。
基于上述发现,研究人员开发了一种选择性肽,该肽模拟SOX9的关键片段,能够有效破坏YAP与SOX9之间的相互作用。通过体内外实验验证,这种肽抑制剂能够显著抑制YAP驱动的肝细胞癌生长,展示了其在抗癌治疗中的潜在应用价值。
为了验证这些发现,研究团队采用了多种实验方法。首先,他们建立了SOX9敲除细胞系,并通过CRISPR-Cas9系统研究了SOX9缺失对YAP活性的影响。接着,通过RNA测序分析了基因表达谱的变化,并验证了YAP靶基因的表达情况。此外,免疫共沉淀实验进一步确认了SOX9与YAP之间的直接相互作用,并探讨了其分子机制。最后,质谱分析帮助鉴定了YAP的甲基化修饰,验证了其对YAP-SOX9结合的影响。
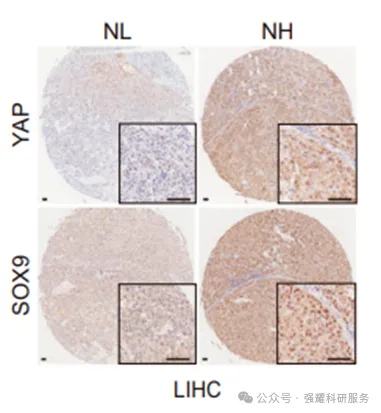
人肝细胞癌(LIHC)肿瘤的YAP和SOX9免疫组化(IHC)染色代表性图像
3、结论与展望
该研究不仅揭示了SOX9作为YAP核转运的重要调节因子的作用,还提出了针对SOX9-YAP相互作用的治疗策略。研究人员通过大量的细胞实验、动物实验以及临床样本分析,验证了肽抑制剂的有效性,为未来开发新型抗癌药物提供了坚实的基础。
总之,这项研究不仅为我们理解YAP核转运机制提供了新的视角,也为抗癌治疗带来了新的希望。随着进一步的研究和临床试验,这一发现有望转化为更有效的肿瘤治疗方法。
本研究中针对Arg-124 (R124) 甲基化YAP的多克隆抗体;用于点印迹分析的多肽;SOX9-HMG结构域相对应的α-螺旋,并在N端融合了细胞穿膜肽(Pep, HLYVSPW)的多肽均由强耀生物合成。


 联系我们
联系我们
 返回
返回