胶质母细胞瘤(GBM)是一种高度侵袭性的脑肿瘤,依靠失调的脂质代谢来促进其生长和侵袭性。中国药科大学联合上海交通大学医学院的研究团队在Chemical Engineering Journal发表了题为“Lipoprotein-mimicking nanodiscs for precise glioblastoma therapy and immune microenvironment modulation”的研究论文,成功构建了一种脂蛋白模拟纳米递送系统PTX-LND@ApoE4,该系统通过穿透BBB、靶向肿瘤、调控脂质代谢和重塑免疫微环境等多种机制,在GBM治疗中展现出优异的效果。其创新的仿生设计和多机制协同策略为GBM的治疗提供了新的思路和方法。
创新点
(1)PTX-LND@ApoE4利用LND变形能力和ApoE4介导的靶向来增强大脑递送。
(2)PTX-LND@ApoE4表现出协同和有效的抗肿瘤功效。
(3)PTX-LND@ApoE4调节脂质代谢并刺激抗肿瘤免疫反应。
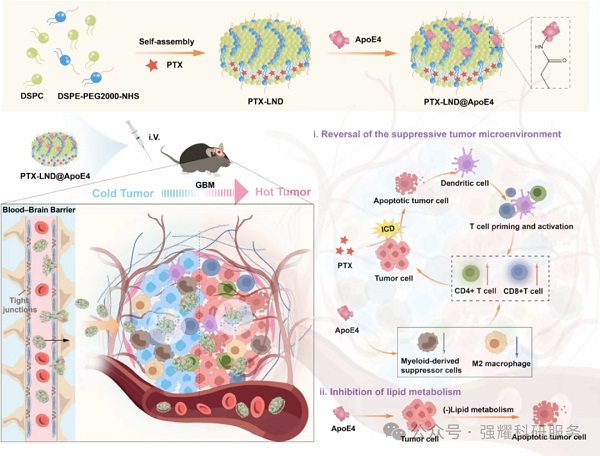
Fig.1 PTX-LND@ApoE4参与肿瘤免疫调节示意图
一、研究背景与目的
胶质母细胞瘤(GBM)是一种高度侵袭性的脑肿瘤,具有生长迅速、侵袭性强、预后极差的特点。
▸GBM特性:依赖异常活跃的脂质代谢维持生长和侵袭,为肿瘤提供了充足的“能量供应”。
▸BBB特性:血脑屏障(BBB)的存在严重限制药物递送,导致传统药物难以有效抵达病灶。
▸ApoE4潜力: 作为脂质运输关键蛋白,可抑制髓系来源抑制细胞(MDSCs)活性,促进NK细胞和CD8⁺T 细胞浸润,调节免疫微环境;同时干扰肿瘤脂质合成。
▸研究目的:构建基于ApoE4和脂质纳米盘(LND)的递送系统,解决 ApoE4易降解、BBB穿透差的问题,实现GBM精准治疗。
二、研究内容与思路

三、研究结果与分析
1.PTX-LND@ApoE4的设计与表征
(1)构建方法:通过乙醇注入法制备载PTX的LND,再与ApoE4共价结合(NHS与氨基反应)。
(2)关键验证:经TEM、DLS、SDS-PAGE、FTIR等证实结构与结合成功,CD光谱显示ApoE4二级结构保留。
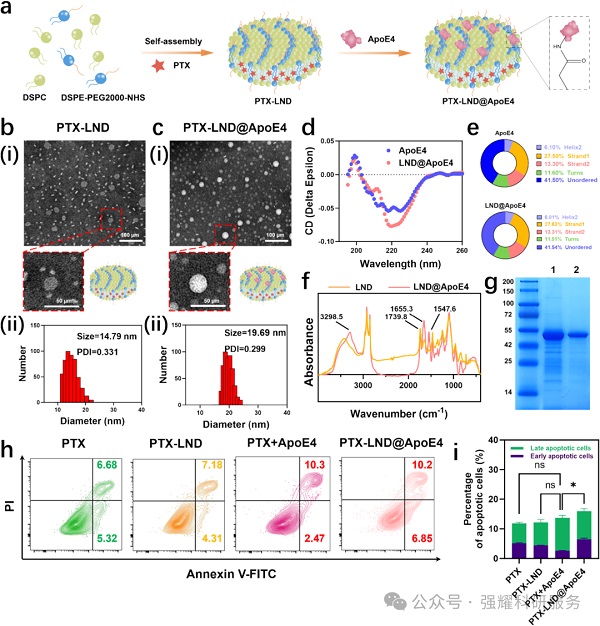
Fig. 2 PTX-LND@ApoE4 的合成示意图
2.体外实验结果
(1)细胞毒性与凋亡:PTX-LND@ApoE4对GL261细胞的杀伤效果优于游离PTX、PTX-LND及PTX+ApoE4,凋亡率显著提高;ApoE4单独处理使GL261的IC50为2.15 μM(正常细胞HEK293T为10.01 μM),且诱导S期阻滞。
(2)BBB穿透能力:在bEnd.3细胞构建的体外BBB模型中,DiD-LND@ApoE42h和4h的穿透效率显著高于DiD-LND和脂质体,因ApoE4降低紧密连接蛋白ZO-1表达,结合LND的可变形结构。
(3)肿瘤球穿透:在GL2613D肿瘤球中,C6-LND@ApoE4穿透深度达80-100μm,优于LND(40-60μm)和脂质体(20-40μm)。
(4)机制验证:qRT-PCR显示其下调脂质合成基因(如SREBF2、HMGCR),上调IL-17信号相关基因(如IL-6、Cxcl2)。
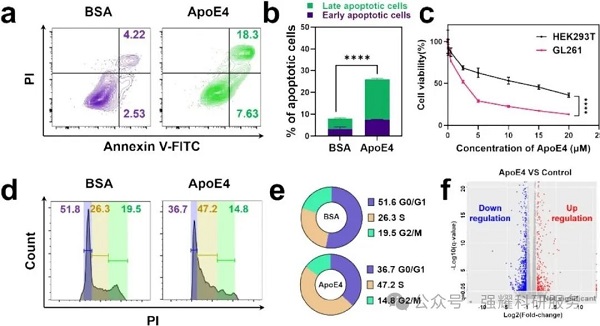
Fig. 3 ApoE 4可诱导GBM细胞凋亡
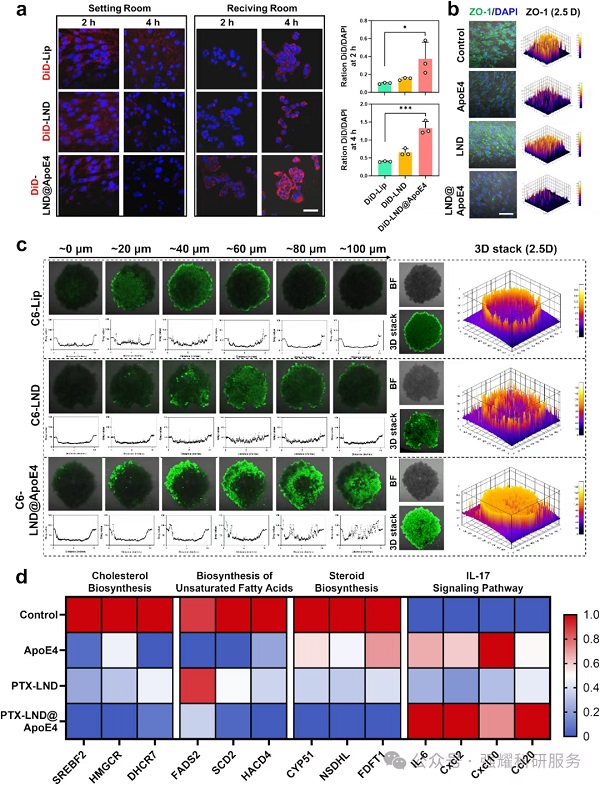
Fig. 4 LND@ApoE4的BBB和胶质瘤穿透性能
3.体内实验结果
(1)生物分布:DiD-LND@ApoE4在颅内GL261荷瘤小鼠脑内24h积累量是DiD-LND的近2倍,且在肿瘤区域富集显著。
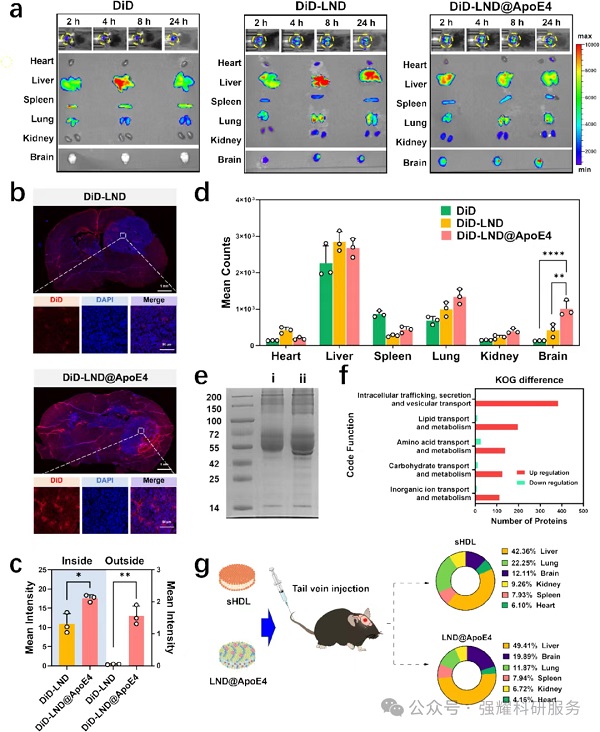
Fig. 5 LND@ApoE4的体内生物分布和胶质瘤蓄积
(2)治疗效果:在原位GBM模型中,PTX-LND@ApoE4处理14天后,肿瘤生物发光强度显著低于其他组,Ki67⁺细胞减少,TUNEL⁺细胞增加,体重下降延迟。
(3)安全性:小鼠肝肾功能指标(AST、ALT、BUN、CRE)无异常,主要器官无病理损伤。
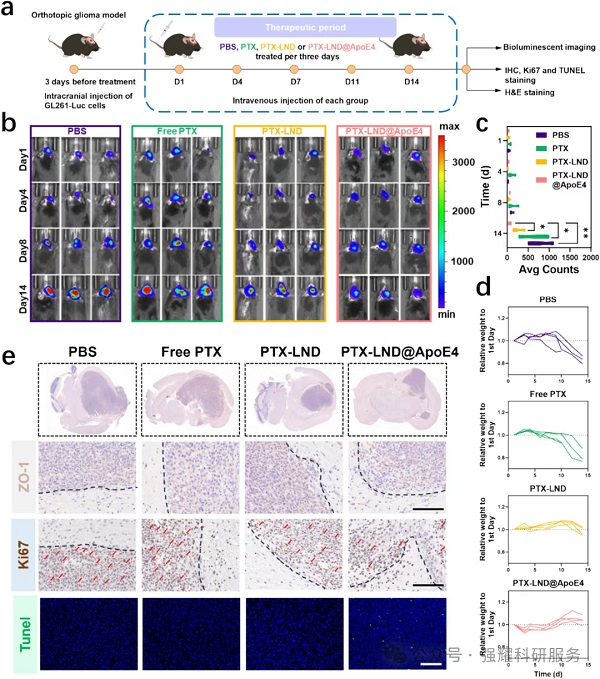
Fig. 6 PTX-LND@ ApoE 4的体内抗GBM功效
4.免疫微环境调节
(1)免疫细胞变化:减少MDSCs(尤其是粒细胞型)和耗竭CD8⁺T细胞(PD-1⁺);增加M1型巨噬细胞(F4/80⁺CD206⁻)、CD4⁺T细胞和细胞毒性CD8⁺T细胞。
(2)机制:激活IL-17信号通路,促进炎症因子分泌,增强免疫原性细胞死亡(ICD)。
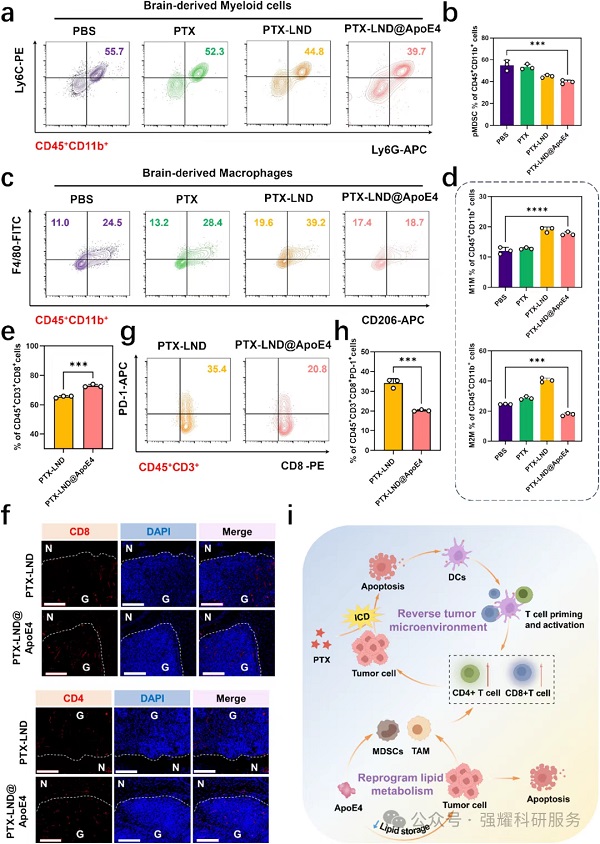
Fig. 7 ApoE 4修饰的PTX-LND用于GBM组织中的免疫调节
四、总结与展望
本研究针对胶质母细胞瘤(GBM) 开发了一种脂蛋白模拟纳米递送系统PTX-LND@ApoE4,该系统由载有紫杉醇(PTX)的脂质纳米盘(LND)与重组ApoE4蛋白结合而成。其利用LND的可变形结构和ApoE4的特性实现高效血脑屏障(BBB)穿透及胶质瘤靶向,通过抑制肿瘤脂质代谢(如下调胆固醇合成基因)和重塑免疫微环境(减少MDSCs、促进M1巨噬细胞极化及细胞毒性CD8⁺T细胞活化),在体内外显著抑制GBM生长。其创新的仿生设计和多机制协同策略为GBM的治疗提供了新的思路和方法。
本研究中重组ApoE4蛋白及其质粒由强耀生物提供;强耀生物提供多肽合成,蛋白和抗体制备等优秀服务助力科研


 联系我们
联系我们
 返回
返回