尽管2023年的生物医药行业面临着诸多变化及挑战,但美国FDA批准的新药仍创5年新高。本文主要根据网上公开内容和各大网站的资料进行收集整理。
1. FDA批准的新药
FDA旗下的药物评估和研究中心(CDER)批准了55款创新药(不含基因疗法和细胞疗法),远超2022年,药物数量仅次于2018年的59款。
获批药物类型上,种类多元化。主要包括新分子实体(38款)和生物制品(17款)。新分子实体中,小分子药物占比最高,其余包括多肽和核酸类药物;生物制品中,抗体占比最高(71%),其中8款单抗、4款双抗,其余是酶类药物。
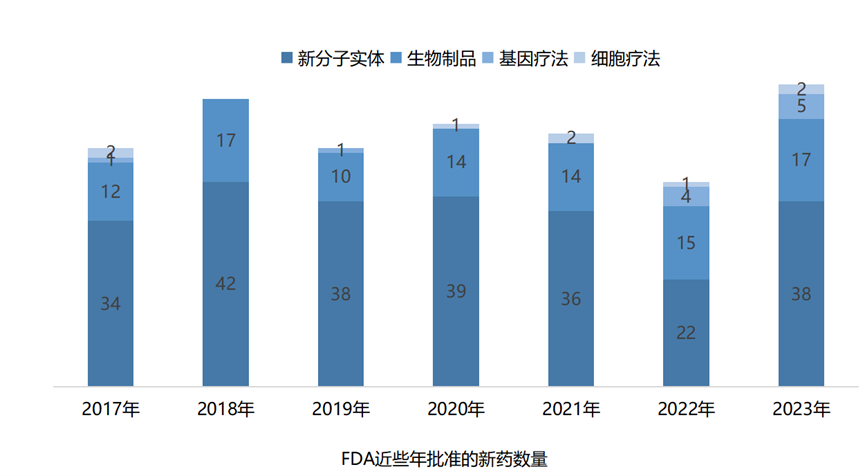
图源:医药魔方
获批药物治疗领域上,适应症类型众多。主要涉及肿瘤、罕见病、传染病、心血管疾病、中枢神经系统疾病、代谢等领域;其中批准的新药数量多集中在肿瘤和罕见病上。
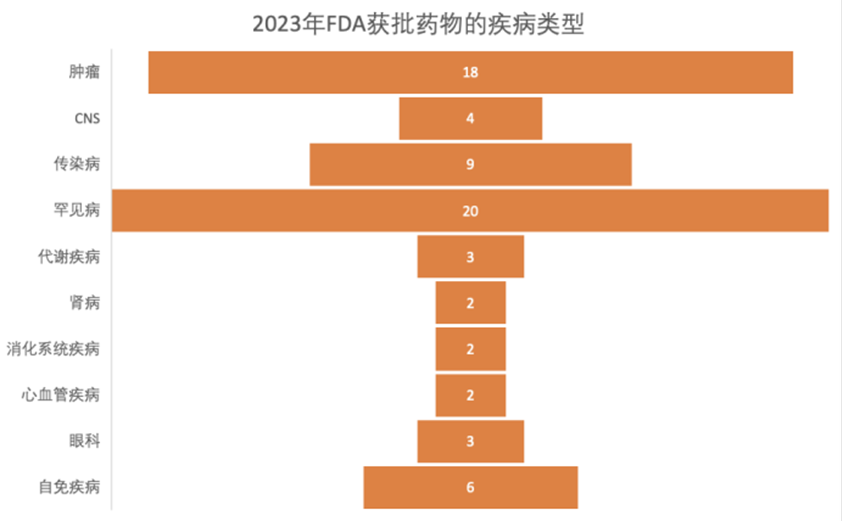
图源:动脉网
2. FDA首款批准药物
(1)首个完全批准的AD新药:Leqembi
Leqembi(lecanemab)是抗Aβ单克隆抗体,用于治疗阿尔茨海默病(AD)。它是20年来首款获得FDA完全批准的AD新疗法,通过静脉(IV)输注给药,选择性结合以中和消除可溶性、有毒的Aβ聚集体(原纤维)。
(2)首个非共价BTK抑制剂:Jaypirca
Jaypirca(pirtobrutinib)是一款非共价、具有高度选择性的布鲁顿酪氨酸激酶(BTK)抑制剂,用以治疗复发/难治性套细胞淋巴瘤(MCL)患者。它可以在先前使用过共价BTK抑制剂(包括伊布替尼、阿卡替尼或泽布替尼)治疗的MCL患者中重建BTK抑制,并延长靶向BTK途径的益处。
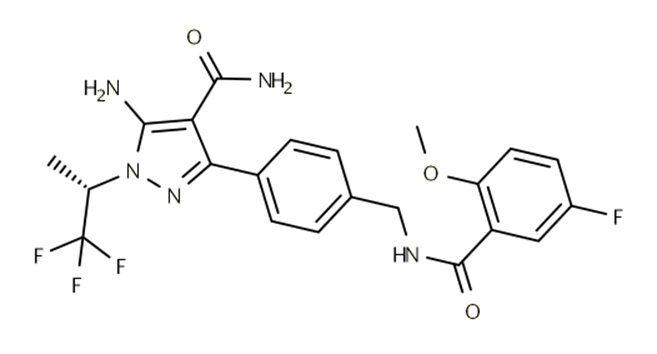
Jaypirca结构图
(3)首个治疗FA的药物:Skyclarys
Skyclarys(omaveloxolone)一款Nrf2激动剂,用于治疗弗里德赖希共济失调症(FA)患者的药物。Nrf2是一种转录因子,通过恢复线粒体功能、减少氧化应激和抑制促炎信号来促进炎症消退。
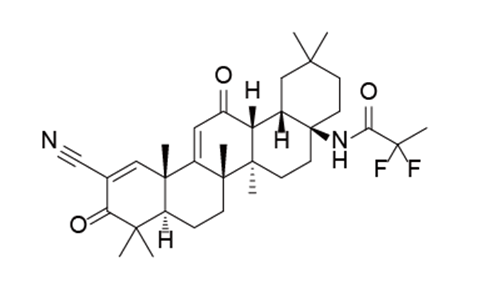
Skyclarys结构图
(4)首个靶向ALS的基因疗法:Qalsody
Qalsody(tofersen)是一种反义寡核苷酸(ASO)药物,用于治疗具有超氧化物歧化酶1突变的肌萎缩侧索硬化(SOD1-ALS)。它可以与编码SOD1的mRNA结合,使其被核糖核酸酶降解,从而减少SOD1蛋白的产生。
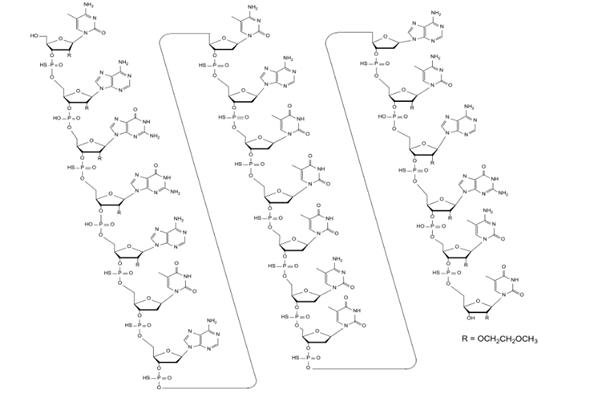
(5)首个口服粪便微生物疗法:Vowst
Vowst(SER-109)是一种基于微生物群的口服胶囊治疗药物,用于预防复发性艰难梭菌感染(rCDI)。它是从健康人粪便纯化而来,平均含有大约50种细菌,通过重建肠道菌群,抑制艰难梭菌的生长。
(6)首个RSV疫苗:Arexvy
Arexvy是一款针对老年人的呼吸道合胞病毒(RSV)疫苗,用于预防60岁以上成人因RSV感染而造成的下呼吸道疾病(LRTD)。Arexvy RSV疫苗包含重组亚单位预融合RSV F糖蛋白抗原(RSVPreF3),与AS01E佐剂相结合。
(7)首个HA基因疗法:Roctavian
Roctavian是一种一次性基因疗法,用以治疗A型血友病(HA)。Roctavian以AAV5病毒载体,递送表达凝血因子VIII(FVIII)到患者细胞,使患者身体能够自行产生凝血因子,防止或减少出血的发生。
(8)首个GPRC5D/CD3双抗:Talvey
Talvey(talquetamab)是一种双特异性T细胞结合抗体,能同时靶向多发性骨髓瘤(MM)细胞上的GPRC5D和T细胞上的CD3,用于治疗复发或难治性MM。它通过激活CD3阳性T细胞,诱导T细胞对GPRC5D阳性MM细胞进行杀伤。
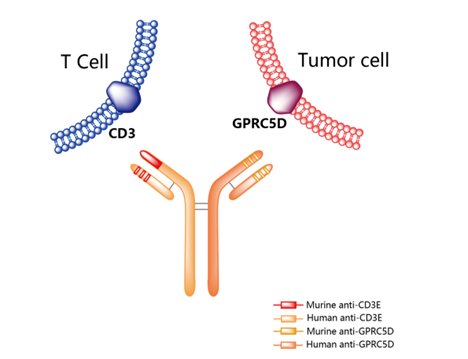
Talquetamab作用机制图
(9)首款口服单药PNH疗法:Fabhalta
Fabhalta(iptacopan)是一种靶向补体旁路途径B因子口服抑制剂,用于治疗成人阵发性睡眠性血红蛋白尿症(PNH)患者。它作用于C5末端通路的上游,同时控制血管内溶血和血管外溶血,弥补了抗C5抗体的不足,同时为患者提供了口服单药的选择。
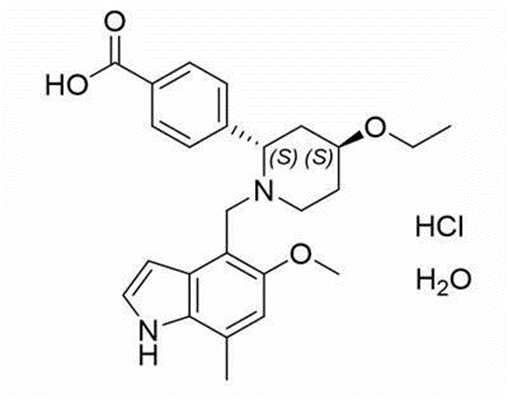
Fabhalta结构图
(10)首个CRISPR基因编辑:Casgevy
Casgevy(exa-cel)是一种自体、体外CRISPR/Cas9基因编辑疗法,用于治疗镰状细胞病(SCD)和输血依赖性β-地中海贫血(TDT)。它通过在体外对患者的造血干细胞进行改造修饰,使红细胞中产生高水平的胎儿血红蛋白(HbF)。
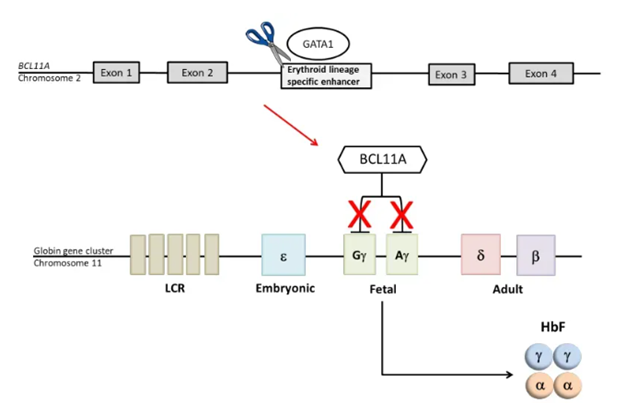
Casgevy的工作原理图
3. FDA批准的多肽类药物
FDA的CDER批准的55款新分子实体药物中含有6款多肽类药物,分别是Daybue、Rezzayo、Paxlovid、Posluma、Aphexda和Zilbrysq。从治疗领域来看,抗肿瘤、抗感染和罕见病领域各有2个。

资料来源:美国FDA官网、博药整理
4. FDA批准的抗体类药物
FDA的CDER批准的8款单抗如下表所示。
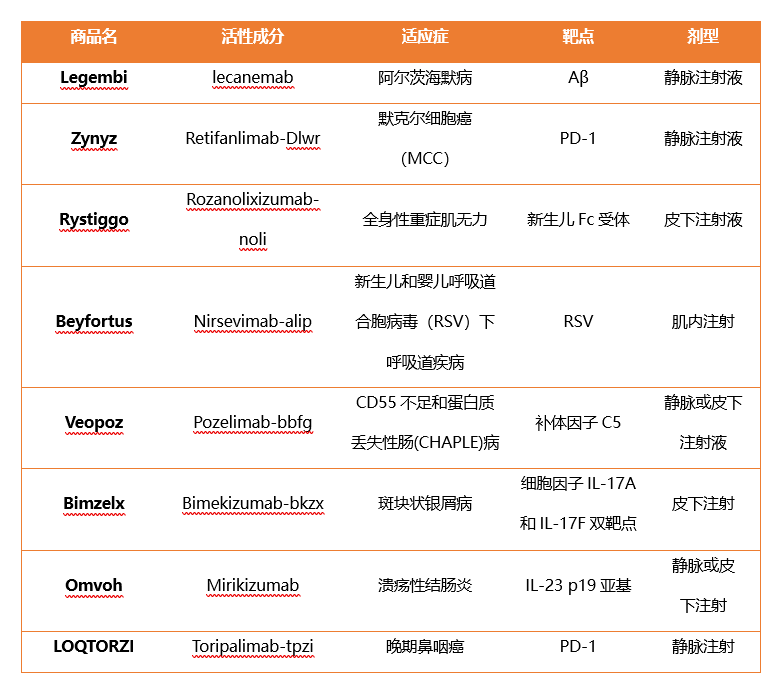
FDA的CDER批准的4款双特异性抗体见下表。
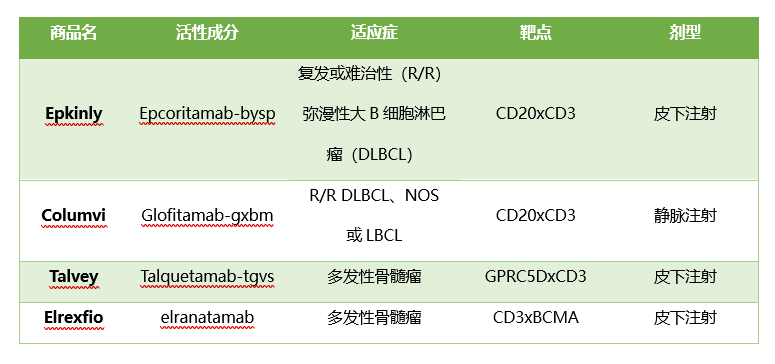
强耀生物15年来为科研机构等提供多肽、蛋白和抗体等一站式服务解决方案,涉及肿瘤、罕见病等领域的研究产品。如果您有相关需求,请随时联系我们。


 联系我们
联系我们
 返回
返回