尽管mRNA疫苗、单克隆抗体和小分子药物在保护人们免受危及生命的COVID-19感染方面发挥了至关重要的作用,但在治疗手段方面仍存在严重不足。目前所缺少的是可以轻松、立即施用、不产生抵抗性的制剂,这类制剂可以在接触这种病毒之前或之后使用,以预防感染或直接减轻症状。
许多高致病性病毒包括冠状病毒,都是利用六螺旋束(6-HB)的七肽重复序列(HR)膜融合机制来实现感染。以冠状病毒为例,SARS-CoV-2表面刺突(S)糖蛋白由S1和S2两个亚基组成。S1亚基负责识别、结合宿主受体ACE2。S2亚基通过HR1和2结构域形成6-HB来介导膜融合。受体结合后,HR1和HR2结构域形成6-HB,该结构将病毒膜和细胞膜拉近以进行融合,从而介导病毒入侵宿主细胞过程。形成6-HB的S2亚基HR结构域α螺旋与其他病毒中的结构域同源,如HIV、呼吸道合胞病毒(RSV)、埃博拉等。
HIV药物如恩夫韦肽(T20)--模仿HIV-1 gp41 HR2结构域,被设计为靶向HR1并破坏6-HB的组装,但其具有成本高、稳定性差等缺点。然后,科学家引入了订书肽修饰HR2肽α螺旋转角,如HIV-1 HR2结构域的双订书肽结构稳定,在体内外均抗蛋白水解,有效靶向HIV-1融合束,抑制HIV-1感染,甚至由于订书肽诱导的结构预折叠,而克服了T20耐药株(即逃逸突变体)。双订书肽RSV F肽,分别通过鼻内和气管内途径给药时,可以防止鼻腔感染和病毒传播到肺部。表明了HR2肽经过改造后可以克服之前的局限性,并进一步应用于呼吸道感染。
1月4日,来自美国Dana-Farber研究院和波士顿大学等研究机构的研究人员试图开发一种基于HR2的局部制剂,以针对SARS-CoV-2和其他可能发生大流行的病毒。相关研究发表在NatureCommunications期刊上,论文标题为:A stapled lipopeptide platform for preventing and treating highly pathogenic viruses of pandemic potential。研究开发的订书脂肽可以阻断一系列SARS-CoV-2变体的感染,经鼻给药后表现出粘膜持久性,稳定性和溶解性显著增强。该订书脂肽也可能对RSV、埃博拉病毒和尼帕病毒等危险和潜在的致命病毒有效。

研究结果
(1)研究团队设计了一个订书脂肽文库,开发数十种用于抗病毒测试的订书肽融合抑制剂。通过改变订书肽位置和PEG长度(订书肽与脂质之间的连接物)开发一种最有效地抑制最广泛的SARS-CoV-2变体的化合物。研究表明,订书肽文库中D-订书肽抗病毒活性最强;PEG长度为8及更长显示出最高的抗病毒活性。

SARS-CoV-2订书脂肽抑制剂的设计和筛选图
(2)然后他们结合订书肽位置和PEG长度开发出一种先导化合物,将其命名为RQ-01。研究显示,引入订书肽后,抗病毒活性提高了1.3-1.5倍,而最佳订书肽位置和延长PEG连接体(PEG8)的结合,使总体抗病毒活性提高了24-39倍。RQ-01治疗不会引起细胞毒性,反而能够在病毒抑制后恢复细胞生长。
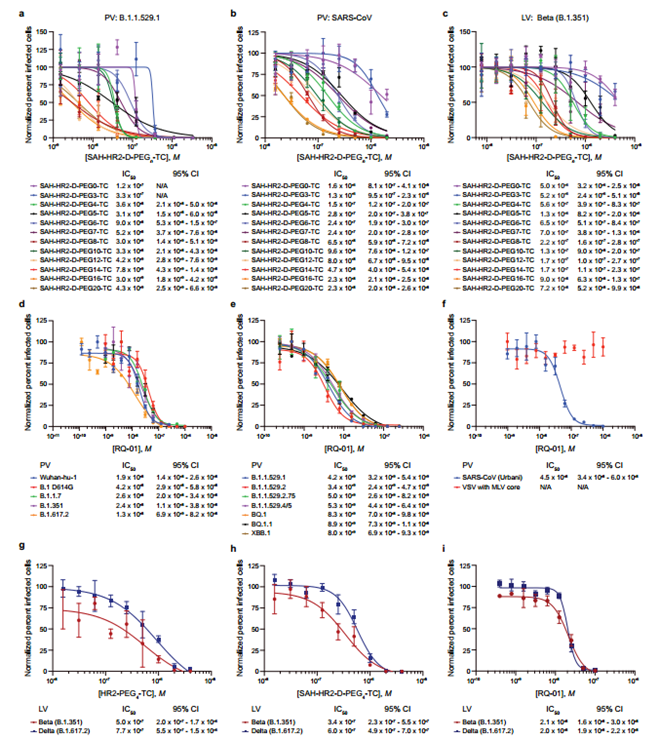
迭代优化得到一种针对SARS-CoV-2变体的先导订书脂肽抑制剂
(3)进一步研究显示:(1)RQ-01的肽序列驱动靶标结合亲和力;(2)脂化显着增强细胞环境中的抗病毒效力;(3)装订在一定程度上有助于靶标结合亲和力和抗病毒效力,更值得关注的是,RQ-01化合物的稳定性和溶解度显著增强。

订书和脂化可单独或联合赋予优异的生物物理和抗病毒特性图
(4)随后,科学家们在仓鼠中评估了RQ-01治疗对预防和治疗SARS-CoV-2的影响。研究表明,RQ-01在对小鼠进行鼻内给药后,可以实现组织持久性。无论是在病毒接种之前还是之后给药,RQ-01都能保护仓鼠免受SARS-CoV-2引起的体重减轻和和肺部损伤。这些结果凸显了RQ-01作为预防和减轻SARS-CoV-2感染症状的有效药物的潜力。

RQ-01在新型冠状病毒感染仓鼠模型中的体内功效图
(5)最后,研究人员将前述流程应用于其他病毒的HR2序列,即RSV、埃博拉病毒和尼帕病毒。研究显示与上述结果类似。
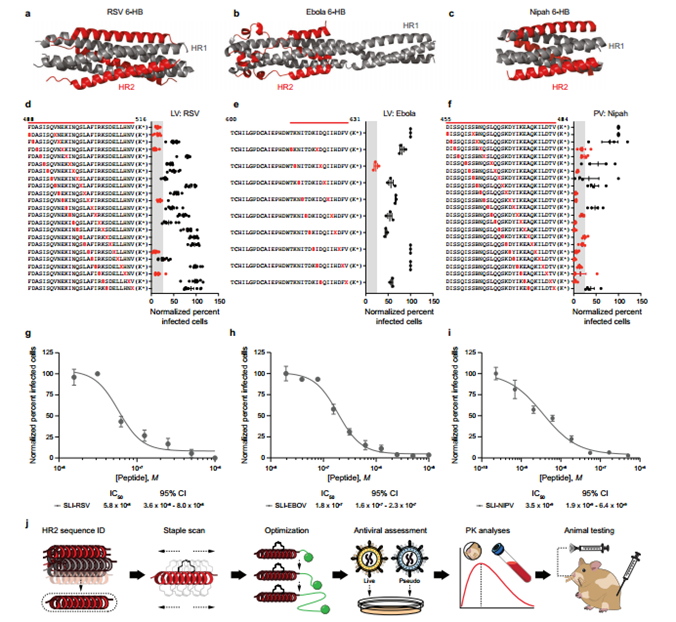
呼吸道合胞病毒、埃博拉病毒和尼帕病毒的先导订书脂肽抑制剂的开发图
该研究的科学家认为,这种方法有可能填补我们抗击COVID-19和其他导致严重呼吸道疾病和出血性疾病的病毒武库中的一个重要空白;还可以促进新一代肽疗法在传染病、糖尿病、癌症和其他疾病等临床应用中的进步。
强耀生物15年来致力于为研究学者们提供多肽、蛋白和抗体等一站式服务,如本文涉及的订书肽及SARS-CoV-2刺突蛋白的受体结合域均可提供。如果您有相关需求,请随时联系我们。


 联系我们
联系我们
 返回
返回