近日,第四军医大学西京医院骨科和西南医科大学的研究团队发表关于线粒体编码肽MOTS-c的论文。该研究不仅揭示了线粒体编码肽MOTS-c在膜修复中的关键作用,还为缺血/再灌注损伤的治疗提供了全新的思路。
该项研究发表在影响因子为12.4的《THERANOSTICS》期刊上,题目为Mitochondria-encoded peptide MOTS-c participates in plasma membrane repair by facilitating the translocation of TRIM72 to membrane。以下是这篇论文的详细介绍。
1、研究背景与目的
在肌肉收缩期间,特别是在离心运动时,细胞膜会受到损伤。此外,肺毛细血管在渗透压变化和通气过程中也会经历机械拉伸,血管壁还会受到流体剪切应力,这些情况下细胞膜会受损。细胞膜修复受损或缺陷已被证实与肌营养不良、肌病、糖尿病和其他疾病有关。
TRIM72:也称为mitsugumin 53(MG53),参与细胞膜修复的分子机制,存在于骨骼肌、心肌、肺、肾等组织中。在氧化应激下,TRIM72通过C242的二硫键形成寡聚化,并在结合带负电荷的磷脂膜时形成高阶组装,这两者有助于核化小泡并将小泡带到受损的质膜。外源性重组人TRIM72蛋白已被证明可以增强组织再生能力并保护免受缺血/再灌注引起的肌肉损伤。此外, TRIM72是一个关键的节点蛋白,多种蛋白依赖于与TRIM72的相互作用才能发挥膜修复功能。
MOTS-c:由线粒体 DNA(mtDNA)编码的多肽,主要在肌肉和其他器官中表达,具有多种生物学功能,已证明能够穿过细胞膜进入血液,推测 MOTS-c 可能作为线粒体与细胞膜之间的信使,帮助 TRIM72 蛋白转运到受损的细胞膜进行修复。
缺血/再灌注损伤:是指组织在经历一段时间的缺血(血液供应不足)之后重新恢复血液供应时发生的一系列损伤反应。虽然恢复血液流动本应有助于组织修复,但在此过程中却可能引发更严重的细胞损伤和炎症反应。这种现象常见于心脏、大脑等器官中,在心脏病发作、脑卒中等情况中尤为显著。
本文的研究目的是探讨线粒体编码的短肽MOTS-c是否参与了质膜修复及其潜在机制。具体来说,研究旨在确定MOTS-c是否通过促进TRIM72向肌膜的转位来增强膜修复能力,并进一步探究这种机制在缺血/再灌注损伤中的作用。
2、研究内容
为了验证MOTS-c在膜修复中的作用及其与TRIM72的相互作用,研究团队进行了多项实验。
首先,他们研究了人类参与者中MOTS-c水平与线粒体丰度及膜修复分子TRIM72之间的正相关性。随后,通过建立高、中强度运动模型,探讨了MOTS-c在膜修复中MOTS-c是否作为线粒体与质膜修复之间的介质。此外,还探讨了MOTS-c在促进膜修复中的作用及其对TRIM72的影响。
接着,通过体外实验验证了MOTS-c对低渗溶液诱导的膜损伤的缓解作用。通过动态膜修复实验和点印迹分析探究MOTS-c与血浆脂质的相互作用及对囊泡与膜的融合的影响。
最后,评估了MOTS-c对常见临床状况心肌缺血/再灌注损伤的保护作用,并发现了MOTS-c在膜修复中的新作用,涉及MOTS-c/TRIM72的转运和MOTS-c与膜的结合。
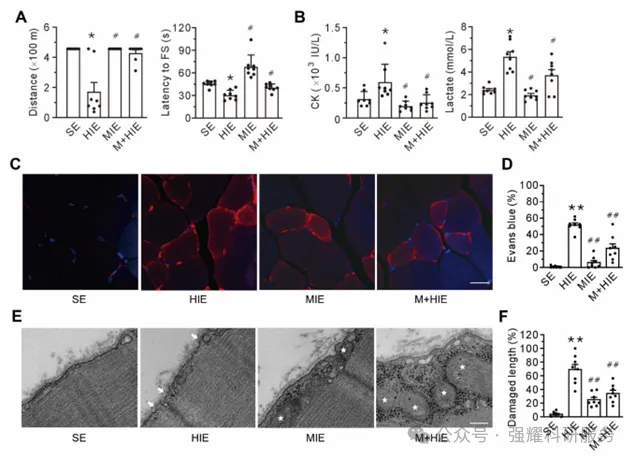
图1 MOTS-c治疗改善高强度运动引起的膜破裂
(A)跑步机成绩。左图为总跑动距离,右图是刺激跑步的第一次电击(FS)的潜伏期。(B)血浆中肌酸激酶(CK,左图)和乳酸(右图)水平分组结果。(C-D)Evans蓝染色的代表性共聚焦图像和Evans蓝阳性细胞百分比的分组结果。从左到右依次为静坐组(SE)、高强度运动组(HIE)、中等强度运动组(MIE)和带 MOTS-c 的高强度运动组(HIE+M)。(E-F)受损膜长度的代表性透射电子显微图和分组结果。箭头表示质膜的纳米孔线粒体。
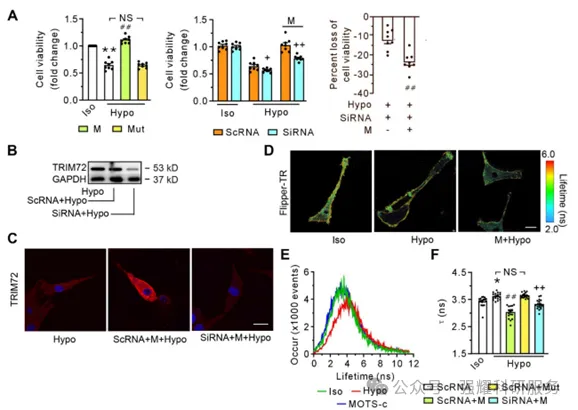
图2 siRNA-TRIM72阻断了MOTS-c在细胞生存力和膜变形性方面的有益作用
(A)不含siRNA-TRIM72(左图)或含siRNA-TRIM72(中、右图)细胞活力分组结果。(B) TRIM72的代表性免疫印迹。(C)siRNA-TRIM72处理或未处理的代表性共聚焦图像。(D) Flipper-TR在等渗溶液或低渗溶液中存在或不存在1µM MOTS-c时的荧光寿命τ1图像。(E) C2C12细胞在低渗溶液中不含或存在1µM MOTS-c时寿命τ1的代表性时间轨迹。(F)寿命τ1平均值分组结果。
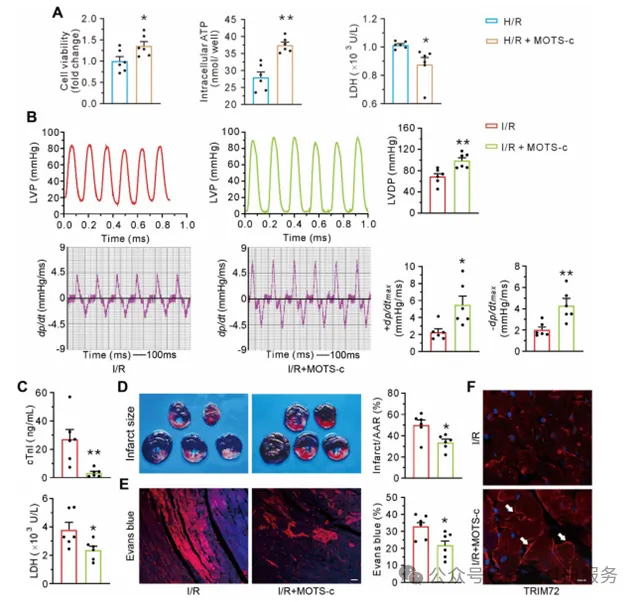
图3 MOTS-c减轻心肌缺血/再灌注损伤
(A)MOTS-c对缺氧-再给氧的新生大鼠心肌细胞的细胞活力、ATP含量和乳酸脱氢酶(LDH)渗漏的影响的分组结果。(B)左心室压力(LVP)和相应的±dp/dtmax的代表性曲线,以及左心室形成压力(LVDP)和±dp/dtmax的分组结果。(C)再灌注结束时血浆中心肌肌钙蛋白I (cTnI)和乳酸脱氢酶(LDH)的分组结果。(D)用氯化三苯基四唑(TTC)染色的心脏切片的代表性图像和梗塞大小的分组结果,梗塞大小以面积的百分比表示风险(AAR)。(E)显示伊文思蓝的细胞内积累和阳性面积分组结果的代表性共聚焦图像。(F) TRIM72的荧光探测的代表性图像。白色箭头表示I/R+MOTS-c组膜募集TRIM72增加。H/R:缺氧/复氧,I/R:缺血/再灌注。
3、研究结果
研究团队首先观察到,适度强度的运动能够显著改善肌肉的膜完整性和身体表现。这一现象伴随着受损肌膜下线粒体数量的增加以及MOTS-c分泌量的升高。进一步的研究表明,MOTS-c通过促进TRIM72向肌膜的转位,有效减轻了缺血/再灌注引起的膜破坏,从而保护了心脏功能。这些发现为通过MOTS-c促进膜修复以挽救器官功能提供了新的治疗策略。
MOTS-c/TRIM72介导的膜完整性改善参与了线粒体触发的膜修复。MOTS-c与血浆脂质的相互作用有助于囊泡与膜的融合。研究者的数据提供了一种新的治疗策略,通过促进膜修复来恢复器官功能。
总之,第四军医大学西京医院骨科的研究团队通过一系列实验,揭示了MOTS-c 在膜修复中的关键作用及其与TRIM72的相互作用机制。这一发现不仅为膜修复领域的研究提供了新的视角,为临床应用提供了新的可能性。特别是在改善器官功能方面的应用。这不仅有望为缺血/再灌注损伤的治疗带来新的突破,也为其他因膜损伤导致的疾病提供了新的治疗方向。
本论文中人源MOTS-c和MOTS-c突变体由强耀生物合成。


 联系我们
联系我们
 返回
返回